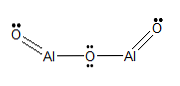
Alumiiniumsulfiid (Al2S3) Keemiline struktuur, nomenklatuur, omadused
The alumiiniumsulfiid (Al2S3) on helehall keemiline ühend, mis on moodustatud metalli alumiiniumi oksüdeerimise teel, kaotades viimase energia taseme elektronid ja muutudes katiooniks ning vähendades mittemetalset väävlit, võites alumiiniumist saadud elektronid ja muutudes anioon.
Selleks, et see juhtuks ja alumiinium suudaks saada oma elektronid, on vaja esitada kolm hübriidset orbitaalset sp3, mis annavad võimaluse moodustada sidemeid väävli elektronidega.

Alumiiniumsulfiidi tundlikkus veele tähendab seda, et õhus veeauru juuresolekul võib see reageerida alumiiniumhüdroksiidi (Al (OH)) saamiseks.3), vesiniksulfiid (H2S) ja vesinik (H2gaasilised; kui see akumuleerub, võib see põhjustada plahvatuse. Seetõttu tuleb alumiiniumsulfiidi pakend teha õhukindlates mahutites.
Teisest küljest, kuna alumiiniumsulfiidil on veega reaktiivsus, on see element, mis ei lahustu nimetatud lahustis.
Indeks
- 1 Keemiline struktuur
- 1.1 Molekulivalem
- 1.2 Struktuurivalem
- 2 Atribuudid
- 2.1 Füüsikalised omadused
- 2.2 Keemilised omadused
- 3 Kasutamine ja rakendused
- 3.1 Superkondensaatorites
- 3.2 Sekundaarse liitiumaku puhul
- 4 Riskid
- 4.1 Esmaabiprotseduur
- 4.2 Tulekustutusmeetmed
- 5 Viited
Keemiline struktuur
Molekulaarne valem
Al2S3
Struktuurivalem
- Alumiiniumsulfiid.
- Di alumiinium trisulfiid.
- Alumiiniumsulfiid (III).
- Alumiiniumsulfiid.
Omadused
Keemilistel ühenditel on enamasti kahte tüüpi omadusi: füüsikaline ja keemiline.
Füüsikalised omadused
Molaarmass
150,158 g / mol
Tihedus
2,02 g / ml
Sulamistemperatuur
1100 ° C
Lahustuvus vees
Lahustumatu
Keemilised omadused
Alumiiniumsulfiidi üks peamisi reaktsioone on veega, substraadina või põhireagendina:

Selles reaktsioonis võib täheldada alumiiniumhüdroksiidi ja vesiniksulfiidi moodustumist, kui see on gaasi või vesiniksulfiidi kujul, kui see lahustatakse vees. Selle olemasolu tuvastab mädanenud munade lõhn.
Kasutused ja rakendused
Superkondensaatorites
Alumiiniumsulfiidi kasutatakse nano võrgustruktuuride tootmisel, mis parandavad spetsiifilist pindala ja elektrijuhtivust, nii et on võimalik saavutada suur mahtuvus ja energiatihedus, mille rakendatavus on superkondensaatorite kasutatavus..
Grafeenoksiid (GO) - grafeen on üks süsinikdioksiidi allotroopseid vorme - see on toiminud alumiiniumsulfiidi (Al2S3) hüdrotermilise meetodi abil valmistatud nano-montana hierarhilise morfoloogiaga.
Grafeenoksiidi toime
Grafeenoksiidi kui tugiomadused, samuti suur elektrijuhtivus ja pindala muudavad nanorambutandi Al2S3 olema elektrokeemiliselt aktiivne.
CV-spetsiifilised mahtuvuskõverad, millel on täpselt määratletud redokspiigid, kinnitavad nanorambutanide Al-pseudovõimsust.2S3 hierarhiline, püsiv grafeenoksiidis 1 M NaOH elektrolüütides. Kõveratelt saadud spetsiifilised CV mahutavuse väärtused on: 168,97 skaneerimiskiirusel 5 mV / s.
Lisaks on täheldatud head galvanostaatilist tühjenemisaega 903 μs, suurt spetsiifilist mahtuvust 2178,16 voolutihedusel 3 mA / Cm.2. Energiatihedus, mis on arvutatud galvanostaatilise väljalaske põhjal, on 108,91 Wh / kg, voolutihedusel 3 mA / Cm2.
Elektrokeemiline impedants kinnitab seega hierarhilise nano-kolibri elektroodi pseudokapitiivset olemust2S3. Elektroodi stabiilsuskatse näitab, et spetsiifiline mahtuvus on kuni 1000 tsüklit 57,44%.
Katsetulemused viitavad sellele, et nanorambutant Al2S3 Hierarhiline sobib superkondensaatorite rakendustele.
Teisese liitiumi patareides
Eesmärgiga arendada välja suure energiatihedusega liitiumpatarei, alumiinium-sulfiid (Al2S3) aktiivse materjalina.
Algne tühjendusvõimsus mõõdetuna Al-st2S3 oli ligikaudu 1170 mAh g-1 100 mA g-1 juures. See vastab 62% -le väävli teoreetilisest võimsusest.
Al2S3 tal on kehv võime säilitamine potentsiaalses vahemikus 0,01 V kuni 2,0 V, peamiselt laadimisprotsessi või Li ekstraheerimise struktuurse pöördumatuse tõttu..
XRD ja K-XANES analüüsid alumiiniumi ja väävli kohta näitasid, et Al2S3 reageerib pöörduvalt laadimis- ja mahalaadimisprotsessi ajal, samas kui Al südamik2S3 näitas struktuurilist pöördumatust, sest LiAl ja Li2S moodustati Al-st2S3 esialgses allalaadimises ja siis jäid nad nii, nagu nad olid.
Riskid
- Vee kokkupuutel vabastab süttivad gaasid, mis võivad iseenesest põletada.
- Põhjustab nahaärritust.
- Põhjustab tugevat silmade ärritust.
- Võib põhjustada hingamisteede ärritust.
Teave võib sõltuvalt lisanditest, lisanditest ja muudest teguritest erineda.
Esmaabiprotseduur
Üldine ravi
Pöörduge arsti poole, kui sümptomid püsivad.
Eriline ravi
Puudub
Olulised sümptomid
Puudub
Sissehingamine
Võtke ohver väljas. Kui hingamine on raske, varustage hapnikku.
Allaneelamine
Manustada üks või kaks klaasi vett ja kutsuda esile oksendamine. Ärge kunagi alustage teadvuseta inimesele oksendamist ega suu kaudu midagi.
Nahk
Peske kahjustatud piirkonda vee ja kerge seebiga. Eemaldage saastunud riided.
Silmad
Peske silmi veega, vilgates sageli mitu minutit. Eemaldage kontaktläätsed, kui need on olemas, ja jätkake loputamist.
Tulekustutusmeetmed
Süttivus
Mitte süttiv.
Kustutusvahendid
Reageerib veega. Ärge kasutage vett: kasutage CO2, liiva ja kustutuspulbrit.
Võitlusprotseduur
Kasutage täielikku kaitset omavat täismassist hingamisaparaati. Nahale ja silma sattumise vältimiseks kandke rõivaid.
Viited
- Salud y Riesgos.com, (s.f), Tervise, riskide ja keskkonna mõiste, mõisted ja artiklid. Taastatud: saludyriesgos.com
- Alumiiniumsulfiid. (s.f) Wikiwandil. Välja otsitud 9. märtsil 2018: wikiwand.com
- Veebielemendid. (S.f) .Dialumiinium Trisulpfide, taastunud 10. märtsil 2018: webelements.com
- Iqbal, M., Hassan, M., M., Bibi.S., Parveen, B. (2017). Sünteesitud grafeenoksiidi baasil põhineva hierarhilise Al2S3 nanorambutaani kõrge spetsiifilise võimsuse ja energia tihedus superkondensaatori rakendamiseks, Electrochimica Acta, Köide 246 ,Lehekülgi 1097-1103
- Senoh, H., Takeuchi, T., Hiroyuki K., Sakaebe, H., M., Nakanishi, K., Ohta, T., Sakai, T., Yasuda, K. (2010). Liitiumis kasutatava alumiiniumsulfiidi elektrokeemilised omadused.Energiaallikate ajakiri,195. köide, 24. väljaanne, leheküljed 8327-8330 doi.org
- LTS Research Laboratories, Inc (2016), ohutuskaart Alumiiniumsulfiid: ltschem.com