Kaltsiumhüdroksiid valem, omadused, reaktiivsus ja kasutusviisid
The kaltsiumhüdroksiid, tuntud ka kui hüdraatne lubi või leotatud lubi, on anorgaaniline ühend valemiga Ca (OH).2.
Kaltsiumhüdroksiid rakendab polümeerset struktuuri nagu kõik metallhüdroksiidid, mis on identne magneesiumhüdroksiidi (Mg (OH)) omaga.2) tuntud ka kui brucita.
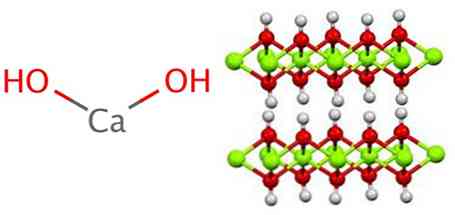
On näha, et selles struktuuris tekivad vesiniku sillad. Kaltsiumhüdroksiid sünteesitakse tööstuslikult, reageerides kaltsiumoksiidi, mida tuntakse ka lubja või lubjana, veega vastavalt järgmisele reaktsioonile:
CaOH + H2O → Ca (OH)2
Samuti valmistatakse see laboris kaltsiumkloriidi ja naatriumhüdroksiidi vesilahuse vahel.
Kaltsiumhüdroksiid esineb looduslikult, kuid harva oma mineraalses vormis portlandiidina, mida leidub mõningates vulkaanilistes ja metamorfsetes kivimites. (Kaltsiumhüdroksiidi valem - kaltsiumhüdroksiidi kasutamine, omadused, struktuur ja valem, 2005-2017).
See ühend on tavaliselt saadaval ka tsemendi-, lahusti- ja tööstuspuhastites (näiteks ehitusmaterjalides), põrandate eemaldajates, tellistest puhastusvahendites, tsemendi paksendustoodetes ja paljudes teistes..
Tavaliselt nimetatakse vesilahust limewater. Lubjavesi valmistatakse, segades kaltsiumhüdroksiidi puhta veega ja filtreerides Ca (OH) liia.2 ei ole lahustunud.
Kui lubjavette lisatakse liigset kaltsiumhüdroksiidi, saadakse kaltsiumhüdroksiidi osakeste suspensioon, mis annab sellele piimjas välimuse, millisel juhul on sellel üldine nimetus lubjapiimast. Lubja piim või küllastunud lubjalahus (lubjavesi) on pH 12,3, mis on põhi-laadi.
Kaltsiumhüdroksiidi füüsikalised ja keemilised omadused
Kaltsiumhüdroksiid on valge või värvitu pulber, mis ei sisalda lõhna. Vesilahuses (küllastunud lahused) on see lahustumatu kaltsiumhüdroksiidi supernatandi tõttu piimjas.
Küllastumata lahused on tavaliselt läbipaistvad ja värvitu lahused, millel on kerge mullane lõhn ja mõru leeliseline kaltsiumhüdroksiidi maitse. Ühendi välimust on kujutatud joonisel fig 3 (Royal Society of Chemistry, 2015).

Kaltsiumhüdroksiidi molekulmass on tahkes olekus 74,093 g / mol ja tihedus 2,211 g / cm3. Selle sulamistemperatuur on 580 kraadi. See on vees halvasti lahustuv, võimaldades lahustada 1,89 grammi liitri kohta temperatuuril 0 ° C, 1,73 grammi liitri kohta temperatuuril 20 ° C ja 0,66 grammi liitri kohta temperatuuril 100 ° C.
See lahustub glütseroolis ja happelistes lahustes. See on alkoholis lahustumatu (riiklik biotehnoloogia teabe keskus, S.F.).
Kaltsiumhüdroksiid lahustatakse osaliselt vees, et saada lahus, mida nimetatakse limewateriks, mis on mõõdukas alus. Lubjavesi või Ca (OH)2 (aq) See reageerib hapetega, moodustades soolasid ja võib rünnata mõningaid metalle, näiteks alumiiniumi. Lubjavesi reageerib kergesti süsinikdioksiidiga, et moodustada kaltsiumkarbonaat.
Ca (OH)2 + CO2 → CaCO3 + H2O
Nitroparafiinid, nitrometaan, nitropropaan jne moodustavad sooli anorgaaniliste alustega nagu kaltsiumhüdroksiid. Need kuivad soolad on plahvatusohtlikud. Ühend on keemiliselt sarnane naatriumhüdroksiidile (NaOH) või naatriumoksiidile (Na2O). Need neutraliseerivad happed eksotermiliselt, moodustades soolasid ja vett.
Nende materjalide segamine veega võib tekitada ohtlikke soojuse koguseid, kuna alus lahustub või lahjendub. Alused reageerivad teatud metallidega (nagu alumiinium ja tsink), et moodustada metallioksiidid või -hüdroksiidid ja tekitada vesinikku.
Alused võivad käivitada polümerisatsioonireaktsioonid polümeriseeruvates orgaanilistes ühendites, eriti epoksiidides. Tuleohtlikke ja / või toksilisi gaase võib tekitada ammooniumisoolade, nitriidide, halogeenitud orgaaniliste ühendite, erinevate metallide, peroksiidide ja hüdroperoksiididega. Seda tüüpi ühendit kasutatakse sageli katalüsaatorina (Chemical Datasheet CALCIUM HYDROXIDE, S.F.).
Reaktiivsus ja ohud

Kaltsiumhüdroksiid on stabiilne ühend, kuigi see ei sobi tugevate hapetega. See on klassifitseeritud ärritavaks ühendiks ja selle ohtude hulgas võib esile tõsta:
See on söövitav silmad (põhjustavad sarvkesta kahjustust või pimedust) ja nahka (tekitavad põletikku ja villid).
Tolmu sissehingamine tekitab seedetrakti või hingamisteede ärritust, mida iseloomustab põletamine, aevastamine ja köha. Tugev ülemäärane kokkupuude võib põhjustada kopsukahjustusi, lämbumist, teadvusetust või surma. Silma põletikku iseloomustab punetus, ärritus ja sügelus (materjali ohutuskaart Kaltsiumhüdroksiid, 2013).
Korduv kokkupuude silmadega madalal tolmu tasemel võib põhjustada naha ärritust ja lokaalset hävimist või dermatiiti. Korduv tolmu sissehingamine võib põhjustada hingamisteede ärritust või kopsukahjustusi.
Kui see kemikaal satub silma, tuleb neid koheselt pesta suure koguse veega, tõstes aeg-ajalt alumist ja ülemist silmalaugu. Pöörduda koheselt arsti poole. Kontaktläätsed ei tohiks selle kemikaaliga töötamisel kasutada.
Kui see kemikaal nahaga kokku puutub, tuleb seebi ja veega saastunud nahk kohe loputada. Kui see kemikaal tungib riietesse, eemaldage kohe riided ja loputage nahka veega. Kui ärritus pesta pärast pesemist, pöörduge arsti poole.
Suure koguse kemikaali sissehingamisel tuleb kokkupuutunud isik kohe värske õhu kätte viia. Kui hingamine on peatunud, tehke taas suu-suhu taaselustamine, hoides ohvrit soojas ja puhkeasendis. Pöörduda arsti poole niipea kui võimalik.
Allaneelamisel pöörduda viivitamatult arsti poole ja võimaluse korral näidata pakendit või etiketti (kaltsiumhüdroksiidi mürgistus, 2017).
Käitlemine ja ladustamine
- Ühendit tuleb hoida kuivas mahutis.
- Ärge sööge ega hingake tolmu sisse.
- Sellele tootele ei tohi kunagi vett lisada.
- Ventilatsiooni puudumise korral tuua piisavad hingamisaparaadid.
- Vältida aine sattumist nahale ja silma.
- Hoida eemal kokkusobimatutest hapetest.
- Hoida pakend tihedalt suletuna.
- Hoida pakend jahedas ja hästi ventileeritud kohas. Mitte hoida temperatuuril üle 25 kraadi.
Kasutused ja rakendused

Kaltsiumhüdroksiidi toodetakse suures ulatuses, seda on kerge käsitseda ja see on üldiselt odav, mistõttu on palju märkimisväärseid kasutusalasid ja rakendusi.
Kaltsiumhüdroksiidi oluline kasutamine on nagu flokulant vees ja reoveepuhastuses. See moodustab koheva laetud tahke aine, mis aitab eemaldada veest väiksemaid osakesi, mille tulemuseks on kergem toode.
Seda rakendust võimaldab kaltsiumhüdroksiidi madal hind ja madal toksilisus. Seda kasutatakse ka värske vee raviks vee pH tõstmiseks. Eesmärgiks on, et torud ei korrodeeruks, kui alusvesi on happeline.
Teine suur rakendus on paberitööstuses, kus seda kasutatakse naatriumhüdroksiidi tootmisel. See muundamine on tuntud kraftprotsessi komponent, mida kasutatakse tselluloosi ekstraheerimisel.
Elukindlustussüsteemides, nagu süsinikdioksiidi pesumasin, eriti suletud ahelaga sukeldumis-re-respiraatorites, kus liitiumhüdroksiidi, mis on enam söövitav, peetakse liiga ohtlikuks.
Seda kasutatakse valgendamise ja krohvimise koostisosana niinimetatud lubjamörtidega. Teedeehituses parandab kaltsiumhüdroksiid pinnase kvaliteeti.
Vastavalt riiklikele tervishoiuinstituutidele kasutatakse tavaliselt hambaravi töös antimikroobse toimeainena kaltsiumhüdroksiidi ja see on valikuline aine, mis moodustab kaitsekihi, mida nimetatakse apikaalseks barjääriks..
Apikaalseid tõkkeid kasutatakse tavaliselt pulpaekroosi vältimiseks olukordades, kus endodontiline kirurgia oleks eriti raske, mis on tavaliselt ebaküpsest püsiva hamba tulemus..
Kuna kaltsiumhüdroksiid võib aidata hammast desinfitseerida, kui infektsioon on juba olemas, võib seda kasutada lühiajaliseks raviks valu ja põletiku vähendamiseks endodontilise kirurgia ettevalmistamisel (Gottfried Schmalz, 2009).
See toimib merevee lisandina, sest see vähendab atmosfääri CO2 ja vähendab kasvuhooneefekti.
Metallide tootmisel süstitakse lubja heitgaasivoolu, et neutraliseerida happed, näiteks fluoriidid ja kloriidid, enne kui nad vabanevad atmosfääri..
Kaltsiumhüdroksiidi kasutatakse mõnedes juuste lõõgastustoodetes aktiivse leeliselise koostisosana.
Cornelli materjaliuuringute keskuse andmetel võib kaltsiumhüdroksiid sirgeks juuksed sirgendada, sest see purustab disulfiidsidemed, mis ühendavad tsüsteine, aminohappeid, mis esinevad kõrgemates kontsentratsioonides looduslikult lokkis juustes. Nende sidemete purustamine ja nende sulgemine kaltsiumhüdroksiidiga muudab püsivalt töödeldud juuste füüsilist struktuuri.
Bordeauxi segus kasutatakse kaltsiumhüdroksiidi lahuse neutraliseerimiseks ja pikaajaliseks fungitsiidiks.
Seda kasutatakse naftatöötlemistööstuses nafta lisandite (salitsülaadid, sulfidid, fenoolid) valmistamiseks naftakeemiatööstuses erinevate markide tahke õli tootmiseks ning ka keemiatööstuses kaltsiumstearaadi valmistamiseks. . Seda kasutatakse tavaliselt süsinikdioksiidi ja gaasi imendumise uurimiseks.
Kaltsiumhüdroksiidi kasutatakse piduriklotside valmistamisel, kuivade segude valmistamiseks värvimiseks ja kaunistamiseks ning pestitsiidide segude valmistamiseks..
Seda kasutatakse ka kaltsiumilisandina ja pH / karbonaatpuhvrina korallide vesiviljeluse jaoks rifi akvaariumis.
Tegemist on "alternatiivse" loodusliku insektitsiidiga, enamik indekseeruvaid putukaid, mis surevad sellega kokkupuutel, sealhulgas puugid, kirbud, mardikad ja vastsed (Russiver, 2015).
Kaltsiumhüdroksiid on tõhus lahendus karvade eraldamiseks loomade nahast, valmistades seda nahatootmiseks.
Kaltsiumhüdroksiidi ja sooja vee segu tekitab vanni, kus värskeid nahka tuleb leotada kuni neli päeva ja loksutada sageli. See protsess lõdvestab juukseid ja nahka sellisel määral, et seda saab tavaliselt käsitsi eemaldada.
Madala mürgisuse ja põhiliste omaduste pehmuse tõttu kasutatakse toiduainetööstuses laialdaselt lõhustatud lubja, et:
- Suhkrutööstuse suhkruroo või suhkrupeedi toormahla selgitamiseks, alkohoolsete jookide ja karastusjookide töötlemisvett, marinaadid ja muud toidud.
- Tee maisitortillad (aidake sarvkesta kokku). Lubjaga küpsetatud mais konverteeritakse nixtamaliks, mis suurendab oluliselt niatsiini biosaadavust, seda peetakse ka maitsvamaks ja kergemini seeditavaks.
- Puhastage kaltsiumi ja magneesiumkarbonaadi soolalahus soola valmistamiseks toidu- ja farmaatsiatööstuses.
- Toetage puuviljajoogid, nagu apelsinimahl, ja imiku piimasegu (BAUM, 2013).
Viited
- BAUM, J. (2013, 16. august). Kaltsiumhüdroksiidi kasutamine. Välja otsitud aadressilt livestrong.com: livestrong.com.
- Kaltsiumhüdroksiid valem - Kaltsiumhüdroksiidi kasutamine, omadused, struktuur ja valem. (2005-2017). Välja otsitud aadressilt softschools.com.
- Kaltsiumhüdroksiidi mürgistus. (2017, 7. veebruar). Välja otsitud medlineplus.gov.
- Keemiline andmeleht CALCIUM HYDROXIDE. (S.F.). Välja otsitud cameochemicals.noaa.gov.
- Gottfried Schmalz, D. A. (2009). Hambaravimaterjalide bioloogiline ühilduvus. Berliin: springer.
- Kemikaali ohutuskaart Kaltsiumhüdroksiid. (2013, 21. mai). Välja otsitud sciencelabist: sciencelab.com.
- Riiklik biotehnoloogia teabekeskus. (S.F.). PubChem Compound andmebaas; CID = 6093208. Välja otsitud aadressilt pubchem.ncbi.nlm.nih.gov.
- Royal Society of Chemistry. (2015). Kaltsiumhüdroksiid. Välja otsitud ChemSpiderist: chemspider.com.
- Russiver, M. (2015, 17. august). Milleks kasutatakse kaltsiumhüdroksiidi? Välja otsitud aadressilt quora: quora.com.


