Naatriumbensoaadi struktuur, omadused, süntees, kasutusalad ja riskid
The naatriumbensoaat on orgaaniline sool, mille keemiline valem on C6H5COONa. Seda toodetakse või genereeritakse bensoehappe ja naatriumhüdroksiidi vahelise neutraliseerimisreaktsiooniga. Tulemuseks on valge tahke aine (alumine pilt), mis lahustub vees ja laguneb kuumutamisega 120 ° C juures.
Seda soola võib leida loomulikult erinevatest puuviljadest ja muudest köögiviljaosadest, nagu mustikad, ploomid, rosinad, kaneel, nelk ja õunad. See on ka vetikate ja taimede metaboliit.

Naatriumbensoaat ei kogune organismis, kuna see ühendab kiiresti aminohappe glütsiiniga, moodustades hippuurhappe, mis eritub vabalt uriiniga..
Seda ühendit kasutatakse koos toidu säilitusainega, mille toime on happelise pH juures tõhusam. See on tingitud orgaaniliste hapete olemasolust, mis annavad toidule naatriumbensoaadi toimimiseks sobiva pH; mis omakorda lõpeb bensoehappega protoonimisega.
Seda soola kasutatakse ka uurea tsükli pärilike ainevahetushäirete raviks, mis tekitab vahepealse metaboliidi akumuleerumise, mille puhul see protsess on puudulik.
Keemilise ohutuse rahvusvaheline programm ei leidnud naatriumbensoaadi kahjulikku mõju inimestele tarbimiseks vahemikus 647–825 mg / kg kehamassi kohta..
Siiski on teatatud, et naatriumbensoaat võib põhjustada pseudoallergilisi reaktsioone ja sümptomeid patsientidel, kellel esineb sageli urtikaaria ja astma episoode..
Indeks
- 1 Naatriumbensoaadi struktuur
- 2 Atribuudid
- 2.1 Keemilised nimetused
- 2.2 Füüsiline kirjeldus
- 2.3 Lõhn
- 2.4 Maitse
- 2.5 Leekpunkt
- 2.6 Isesüttimine
- 2.7 Tihedus
- 2.8 Lahustuvus
- 2.9 Stabiilsus
- 2.10 Lagunemine
- 2,11 pH
- 2.12 Pinna pinge
- 3 Kokkuvõte
- 4 Kasutamine
- 4.1 Toidus
- 4.2 Meditsiiniline ravi
- 4.3 Muu
- 5 Riskid
- 6 Viited
Naatriumbensoaadi struktuur
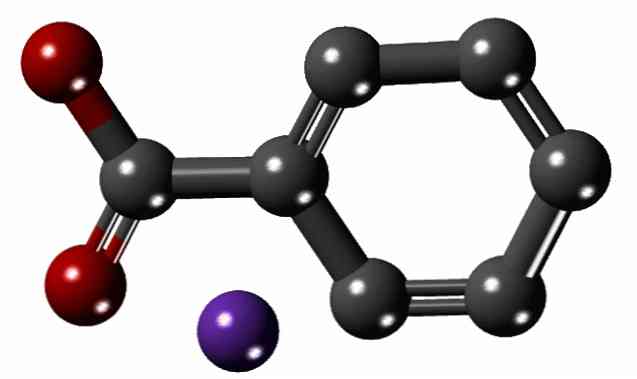
Ülemises pildis on naatriumbensoaadi struktuur näidatud kerakeste ja baaride mudeliga. Aromaatset ringi võib näha palja silmaga karboksülaadi rühmaga -COO-, sellega seotud (punaste sfääride); ja viimane omakorda tõmbab Na katiooni elektrostaatiliselt+ (lilla sfäär).
Kuna kahe iooni suuruse erinevus on suur (võrreldes pildiga), ei ole üllatav, et naatriumbensoaadi kristallide retikulaarne energia on madal. See põhjustab, et nende kristallidel on loomulik kalduvus lahustuda polaarsetes lahustites või kannatada mitmeid keemilisi reaktsioone.
C6H5COO- See võib vastu võtta kaks vesinikilda kahest veemolekulist, mis soosib selle hüdratatsiooni. Vahepeal Na+ Samuti lõpeb see veega solvaadiga, ületades elektrostaatilised jõud, mis hoiavad seda koos C-ga6H5COO-.
Niisiis koosneb see sool C-ioonidest6H5COO- ja Na+, mis on paigutatud korrapäraselt kristallide ehitamiseks. Kirjanduses ei ole saadud teavet selle kristalse struktuuri kohta, mistõttu ei ole teada, milline on selle soola ühikuliik.
Omadused
Keemilised nimetused
-Naatriumbensoaat
-Bensoehappe naatriumsool
-Sobenato
-Antimol.
Füüsiline kirjeldus
Valged graanulid või kristalne pulber. Värvitu kristalne pulber.
Lõhn
Tualettruum.
Maitse
Bittersweet, kokkutõmbav ja ebameeldiv.
Süütepunkt
> 100 ° C.
Isesüttimine
> 500 ° C.
Tihedus
1,50 g / cm3.
Lahustuvus
-Lahustub vedelas ammooniumis ja püridiinis.
-Etanoolis veidi lahustub: 8,22 g / 100 g 25 ° C juures.
-Metanoolis on see lahustuvam kui etanoolis: 8,22 g / 100 g 15 ° C juures.
Stabiilsus
See on soovitatavates säilitustingimustes stabiilne. See võib olla niiskuse suhtes tundlik, hüdrolüüsides bensoehappeks. Kokkusobimatu tugevate oksüdeerivate ainete, leeliste ja mineraalhapetega.
Lagunemine
Kuumutamisel lagunemisel temperatuuril 120 ° C (248 ° F) kiirgab see naatriumoksiidi ja muude koostisosade, mis võivad olla mürgised ja kantserogeensed, suitsu..
120 ° C juures lagunemisel takistab see selle keemis- ja sulamispunktide täpsust, kusjuures nende parameetrite väärtused on teoreetilised hinnangud.
pH
Ligi 8, vees lahustunud. See tähendab, et tegemist on aluselise soolaga. Seda seetõttu, et see hüdrolüüsib OH-i ioonide vabastamiseks-.
Pinna pinge
72,9 mN / cm 20 ° C juures 1 g / l lahuses.
Süntees
Naatriumbensoaadi sünteesiga seotud bensoehape valmistatakse peamiselt kolme meetodi abil:
-Naftaleen oksüdeeritakse vanadiinpentoksiidiga, saades ftaalanhüdriidi. See ühend võib läbida bensoehappe dekarboksüülimise, kuna selle kahe aromaatsete tsüklite struktuuris tundub olevat kaks -COO rühma, mis on kondenseerunud.
-Tolueen oksüdeeritakse lämmastikhappe lisamisega bensoehappeks. Selles reaktsioonis oksüdeeritakse metüülrühm "lihtsalt" karboksüülrühmaks:
C6H5CH3 => C6H5COOH
-Lõpuks hüdrolüüsitakse bensotrikosloriid bensoehapet sisaldavate mineraalhapete toimel.
Saadud bensoehape on ükskõik milline neist kolmest meetodist, seejärel lahustatakse naatriumhüdroksiidis. Need ühendid viiakse läbi neutraliseerimisreaktsiooniga, tekitades naatriumbensoaati ja vett.
C6H5COOH + NaOH => C6H5COONa + H2O
Reaktsiooni võib läbi viia ka naatriumkarbonaadiga, kuigi selle saagis võib olla soovitavam.
Kasutamine
Toidus
Naatriumbensoaat on toidu säilitusaine, mis on võimeline pärssima või viivitama käärimisprotsessi, hapestamist või mis tahes protsessi, mis põhjustab nende riknemist. Lisaks on naatriumbensoaadil fungitsiidne toime.
See sool suudab kõrvaldada toiduainetes esinevad pärmid, bakterid ja seened. Selle säilitusaine on pH juures tõhusam < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Naatriumbensoaati kasutatakse ka gaseeritud jookide ja karastusjookide säilitamiseks, milles on süsinikhapet. Samuti on sidrunhappes rikas ja üldiselt happelises keskkonnas leiduvate hapetega toiduainetes.
Lisaks kasutatakse seda söödas naatriumbensoaadi kontsentratsiooniga 0,1%. Kasutatava bensoehappe ja naatriumbensoaadi maksimaalne kogus toiduainetes ei ületa 2000 mg / kg toidu kohta.
Meditsiiniline ravi
Äge hüperammoneemia
Naatriumfenüülatsetaati ja naatriumbensoaati kasutatakse adjuvantravi vormis akuutse hüperammoneemia ja sellega seotud entsefalopaatia raviks uurea tsükli muutustega patsientidel..
Need ühendid on klassifitseeritud harva kasutatavateks ravimiteks. See nimetus kehtib ravimite kohta, mis ei ole majanduslikust seisukohast kasumlikud.
Skisofreenia
Skisofreenia ravis on eksperimentaalselt kasutatud naatriumbensoaati. Uuringu keskne osa on roll, mis ravis täidab D-aminohapete oksüdaaside ensüümide pärssimist, naatriumbensoaadi aktiivsust..
Arginosuktsiinhappeauria
Naatriumbensoaati kasutatakse argininosuktsinhappe happe raviks, mis on pärilik metaboolne häire, mis võib põhjustada patsientidele ammoniaagi kontsentratsiooni suurenemist, mis on võimeline mõjutama kesknärvisüsteemi..
Inhibiitor
-See on ensüümi araquidonato 15-lipoksügenaasi inhibiitor, ensüüm, mida farmaatsiatööstus uurib südame isheemiatõve raviks.
-See pärsib lipaasi ensüümi triatsüülglütseriidide, ensüümi, mis põhjustab glütserooli ja rasvhapete vabanemist peensooles, mõju, võimaldades seega nende lipiidide imendumist toidus..
Võib olla võimalik kasutada naatriumbensoaati lipiidide, nagu triatsüülglütseriidide, soole imendumise reguleerimiseks..
Pärilikud häired
Naatriumbensoaati kasutatakse mitmete pärilike haiguste raviks, mis on seotud aminohapete metabolismiga, mille hulgas on mainitud: hüpererginineemia ravi ja ornitiini ensüümi translokaasi puuduse ravi..
Teised
-Seda kasutatakse alkoholipõhistes loputustes ja hõbeda poleerimises. Lisaks sellele kasutatakse seda pürotehniliste ühendite väljatöötamisel, vastutades süüte eest, mis tekib süütamise ajal.
-Seda kasutatakse korrosioonivastase ainena, mis on üks peamisi nõudmisi selle soola tootmisel. Seda kasutatakse ka jahutusvedelikes, antifriisides ja teistes veepõhistes süsteemides.
-Plastide, nagu polüpropüleen, koostises kasutatakse selle tugevust ja selgust.
-Serveerib stabilisaatorina vannitubades ja fotograafias.
Riskid
FDA klassifitseerib naatriumbensoaadi "üldiselt ohutuks" doosina 0,1% toidu massist. Seda ei peeta ärritavaks nahale ja silma, seega võib öelda, et äge mürgisus on väike.
Siiski võib naatriumbensoaat põhjustada kokkupuutel mitteimmunoloogilisi reaktsioone (pseudoalleriat). See toime on haruldane inimestel harva, kuid urtikaaria või astma sümptomite sagedaste episoodidega patsientidel võib nende sümptomite esinemissagedus suureneda..
Rottide ja hiirtega läbiviidud uuringutes ei leitud naatriumbensoaadi kantserogeenset toimet.
On juhitud tähelepanu ebamugavusele selle kasutamisel askorbiinhappe juuresolekul, mis võib toota benseeni; mürgine ühend, mida nimetatakse kantserogeenseks.
Viited
- Net Industries. (2019). Naatriumbensoaadi tootmine. Välja otsitud andmebaasist: science.jrank.org
- Wikipedia. (2019). Naatriumbensoaat. Välja otsitud andmebaasist: en.wikipedia.org
- PubChem. (2019). Naatriumbensoaat. Välja otsitud andmebaasist: pubchem.ncbi.nim.nih.gov
- Hanes T. (2019). Faktid naatriumbensoaadi kohta. Livestrong. Välja otsitud andmebaasist: livestrong.com
- Keemiline raamat. (2017). Naatriumbensoaat. Välja otsitud: chemicalbook.com
- Lane H. et al. (2013) Jama Psichiatry. 70 (12): 1267 - 1275.
- Maailma Terviseorganisatsioon Genf. (12. aprill 2005). Bensoehape ja naatriumbensoaat. [PDF] Välja otsitud andmebaasist: who.int


