Grami värvi alus, materjalid, tehnika ja kasutusalad
The Grami värv on kõige lihtsam ja kõige kasulikum värvimistehnika diagnostilises mikrobioloogias. Selle meetodi on loonud Taani arst Hans Christian Gram 1884. aastal, kes suutis klassifitseerida bakterid grampositiivsesse ja gramnegatiivse, vastavalt rakuseina koostisele.
Huckeri poolt tehtud tehnikat muudeti 1921. aastal reagentide stabiliseerimiseks ja pleki kvaliteedi parandamiseks, nii et Grami värv on tuntud ka kui Gram-Hucker.
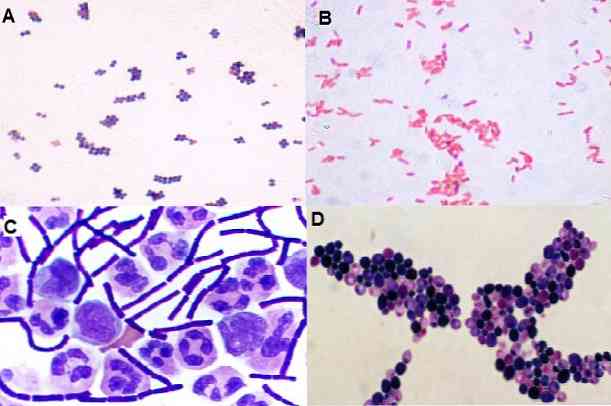
Selle tehnikaga on võimalik jälgida ka mikroorganismide vormi, st kas need on kookid, batsillid, kokkobatsillid, pleomorfsed, filamentsed. Lisaks selle levikule ruumis: klastris, ahelas, isoleeritud, paaridena, tetradides jne..
Bakteriaalse infektsiooni kahtluse korral tuleks enamik saadud proove levitada slaidile ja värvida mikroskoobi all uurimiseks grammiga..
Grami aruanne annab arstile ülevaate sellest, millist tüüpi mikroorganism võib olla nakkuse põhjuseks, enne saagi lõpliku tulemuse saamist.
Mõnel juhul on patsiendi elu väga ohtlik, seega vajavad arstid tungivalt Grami aruannet, et panna empiiriline ravi, oodates mikroorganismi tuvastamist.
Näiteks kui gramm näitab, et tserebrospinaalvedelikus on grampositiivseid kokteile, suunab arst esialgse ravi antibiootikumidega, mis seda tüüpi baktereid kõrvaldavad, vastavalt sellele kehtestatud protokollidele..
Kui lõpptulemus on eraldatud mikroorganismi ja selle vastava antibiootikumi nimega, hindab arst, kas ravi tuleb muuta või mitte. See otsus tehakse vastavalt uuringule, mis käsitleb mikroorganismi vastuvõtlikkust antibiootikumidele, mida ta saab, ja patsiendi evolutsiooni..
Indeks
- 1 Sihtasutus
- 2 Materjalid
- 3 Värvide ja reaktiivide valmistamine
- 3.1 Kristallviolettlahus
- 3.2 Jodo-Lugol
- 3.3 Pleegitamine
- 3.4 Kontrast
- 4 Reaktiivide säilitamine
- 5 Värvitava proovi leviku ettevalmistamine
- 5,1-otseste proovide gramm
- 5.2. Põllukultuuride gramm
- 6 Tehnika
- 7 Utiliit
- 8 Üldised vead
- 9 Viited
Sihtasutus
Tegemist on tehnikaga, mis esitab 4 põhilist sammu: värvimist, fikseerimist mordandi, värvimuutuse ja kontratseptsiooniga. Seetõttu eristab see meetod lisaks bakterite värvimisele ka neid.
Kristallviolett on esimene värvaine. Sellel on afiinsus peptidoglükaani suhtes ja lilla värvib kõik olemasolevad bakterid, seejärel asetatakse lugool, mis toimib mordana, st indutseerib kristallviolet-joodi - ribonukleaarsete valkude lahustumatu kompleksi moodustumist rakus..
Grampositiivsed bakterid, millel on paks peptiidoglükaani sein, moodustavad rohkem komplekse (kristallviolet-jood), mistõttu nad säilitavad värvi.
See mõjutab ka seda, et Gram-positiivsete bakterite sein sisaldab rohkem küllastumata happeid, millel on kõrge afiinsus oksüdeerivate ainete suhtes (Lugol).
Vahepeal on gramnegatiivsetel bakteritel peptiidoglükaani õhuke kiht, mis muudab bakterid vähem keeruliseks kui grampositiivsed bakterid.
Seejärel tuleb värvimuutus, kus grampositiivsed ja gramnegatiivsed bakterid käituvad erinevalt.
Gramnegatiivsed bakterid sisaldavad välismembraani, mis sisaldab rohkelt lipopolüsahhariide, mis on selle rakuseina osa. Rasvad hävitatakse alkoholi atsetooniga kokkupuutel, nii et välismembraan on destabiliseeritud, vabaneb violetne kristall.
See on siis värvitud punase värviga safraniini või põhifuksiiniga.
Gram-positiivsete bakterite puhul on nad vastupidavad värvuse muutumisele, sest valgendaja sulgeb poorid, mis takistab kristallviolet / joodikompleksi pääsemist.
Seetõttu on violetse kristalliga värvus stabiilne ja safraniinile või fuksiinile ei ole ruumi. Sellepärast määravad need bakterid intensiivse sinise või lilla värvi.
Materjalid
Grami värvikomplekt koosneb:
- Lilla kristall
- Lugol
- Atsetoonalkohol
- Safraniin või põhifuksiin
Värvide ja reaktiivide valmistamine
Kristallviolettlahus
Lahendus A:
Violetkristall -2 gr
Etüülalkohol 95% -20cc
Lahendus B:
Ammooniumoksalaat -0,8 g
Destilleeritud vesi -80 cm3
Lillakristallide lõplikuks valmistamiseks tuleb 1:10 lahus lahjendada destilleeritud veega ja segada 4 osa lahusega B. Segu hoitakse 24 tundi enne kasutamist. See filtreeritakse paberfiltri abil merevaigu värvimiseks kolvis.
Igapäevaselt kasutatav kogus kantakse tilgutiga merevaigu pudelisse.
Jodo-Lugol
Kaalutakse ja mõõdetakse iga ühendi näidatud kogus järgmiselt:
Iodo kristallid - 1gr
Kaaliumjodiid - 2gr
Destilleeritud vesi -300 cm3
Kaaliumjodiid lahustub vees vähe ja seejärel lisatakse jood. Lahus raseeritakse merevaigukollaseks pudelisse.
Iga päev kasutatav kogus kantakse tilgutiga väiksemale merevaigukollasesse pudelisse.
Pleegitamine
95% etüülalkoholi -50 ml
Atsetoon - 50 ml
See on valmistatud võrdsetes osades. Katke hästi, see kipub aurustuma.
Pange tilgutiga pudelisse.
See preparaat annab värvi muutuse mõõduka aja jooksul 5-10 sekundit ja on kõige soovitatavam.
Algajad eelistavad kasutada ainult 95% etüülalkoholi, kus värvimuutus on aeglasem 10 kuni 30 sekundi jooksul.
Kuigi kõige kogenum saab kasutada puhast atsetooni, kus värvimuutus toimub väga kiiresti 1 kuni 5 sekundi jooksul.
Kontrast
Safraniini põhilahus
Safranina -2,5 gr
Etüülalkohol 95% -100 cm3
Pärast kaalumise lõppemist lahustub safraniini kogus 100 cm3 etüülalkoholis 95% -ni.
Töötav safraniini lahus valmistatakse põhilahusest.
Selleks mõõdetakse 10 cm3 põhilahust, lisatakse 100 ml destilleeritud vett.
Soovitatav on kanda igapäevaselt kasutatav kogus kollasesse pudelisse tilgutiga.
Mikroorganismid, mis värvivad Gram-Huckeri peitsiga nõrgalt Gram-negatiivseid, nagu teatud anaeroobid, Legionella sp, Campylobacter sp ja Brucella sp, neid saab palju paremini värvida, kui kasutatakse Kopeloffi poolt Gram-Huckeri värvimiseks tehtud modifikatsiooni, mida nimetatakse Gram-Kopeloffi plekiks..
See meetod muudab safraniini värvi põhifuksiiniga. Selle modifikatsiooniga on võimalik ülalmainitud mikroorganisme efektiivselt värvida.
Reaktiivide säilitamine
Valmistatud värvained tuleb hoida toatemperatuuril.
Proovi ettevalmistamine levis värvi
Proov peab sisaldama vähemalt 10. \ T5 mikroorganismid enne mikroorganismi jälgimist, on tõenäoline. Plaate võib valmistada otsesest proovist või kultuuridest tahkes või vedelas keskkonnas.
Levikud peaksid olema ühtsed, hästi jaotunud ja mitte liiga paksud, et olemasolevaid struktuure paremini visualiseerida.
-Otseste proovide gramm
Uriini gramm ilma tsentrifuugita
Uriini segatakse ja 10 µl asetatakse slaidile. Vähemalt ühe bakteri / immersioonivälja vaatlus näitab, et nakkus on olemas.
See tähendab, et kultuuris on ligikaudu 100 000 CFU / ml (10. \ T5 85% juhtudest.
See meetod ei ole kasulik kolooniate arvu alla 100 000 CFU.
LCR gramm
CSF tuleks tsentrifuugida, supernatant eemaldada ja pellet levida slaidil. See vedelik on normaalsetes tingimustes steriilne; bakterite jälgimine näitab nakkust.
Gramm hingamisteede proove
Röga Gram, bronhiaalne või bronhokalveolaarne loputus, kuigi võib esineda mitmesuguseid mikroorganisme, on alati diagnoosimisel juhitav, lisaks on täheldatud rakkude tüüp kasulikuks.
Röga puhul tuleb määrdeainet valmistada proovi kõige peenemate osadega.
Stool Gram
Seda tüüpi proovidele ei ole soovitatav Grami teostada, kuna sellel ei ole diagnostilist väärtust.
-Gramkultuurid
Neid saab teha kahel viisil: üks vedelkultuuridest ja teine tahketest kultuuridest.
Vedelad kultuurid
Vedelkultuuridest on see äärmiselt lihtne; kergema valguse all võetakse mitu häguse puljongi röstimist, mis asetatakse puhtale ja kuivale slaidile, andes ringi liikumise keskelt perifeeria suunas, et materjali ühtlaselt jaotada.
Sellel lastakse õhu käes iseeneslikult kuivada. Kui see on kuivanud, kinnitatakse materjal lehele soojusega. Selleks lastakse klambri abil leht 3 3 korda läbi Bunsen-põleti leegi, hoolimata sellest, et materjali ei põletata..
Lehel lastakse jahtuda ja asetatakse värvimissillale.
Tahked kultuurid
Grami värvi laiendamiseks tahkest kultuurist toimige järgmiselt.
Enne kolooniate valimist tuleb valmistada slaid, asetades kaks tilka ligikaudu steriilset füsioloogilist soolalahust..
Kui algne kultuuriplaat sisaldab mitut erinevat tüüpi kolooniaid, valitakse iga grammi isoleeritud koloonia Grami teostamiseks. Iga koloonia võetakse koos plaatina ahelaga, et see lahustuks eelnevalt slaidile kantud soolalahuses.
Tsirkulaarseid liikumisi antakse keskelt perifeeriasse, et jaotada koloonia slaidile ühtlaselt..
Sellel lastakse õhu käes iseeneslikult kuivada. Kui leht on kuivanud, fikseeritakse leht soojusega, nagu ülalpool selgitatud (slaidi süütamine kergemaga), olles ettevaatlik, et materjali ei põletaks.
See protseduur tuleb läbi viia iga eri tüüpi kolooniaga. Paberil tuleb märkida täheldatud järjekord, näiteks:
Koloonia 1: Kollane beeta-hemolüütiline koloonia: klastrites täheldati grampositiivseid kokteele
Koloonia 2: kreemikoloonia ilma hemolüüsita: täheldati gramnegatiivseid kokkobatsilli.
Iga leht peab olema märgistatud, et teada saada, mida me jälgime.
Tehnika
Gramma värvimise tehnika on äärmiselt lihtne ja suhteliselt odav ning seda ei saa mikrobioloogia laboris mööda lasta.
Sama tehakse järgmiselt:
- Kinnitage määrdeainega kuumus ja asetage värviline sild.
- Leht on 1 minutiks täielikult kaetud lilla klaasiga.
- Peske veega. Ärge kuivatage
- Katke plaat Lugoli lahusega, jäta 1 minut. Peske veega. Ärge kuivatage.
- Segage 5-10 sekundit, segades kergelt atsetoonalkoholi. Või asetage leht püstises asendis ja tilgutage tilgutit sisaldavat ainet pinnale, kuni allesjäänud lilla klaas on tõmmatud. Ärge ületage.
- Peske veega. Ärge kuivatage.
- Vahetage leht värvilisele sildale ja katke 30 sekundit safraniiniga (Gram-Hucker) või 1 min põhifuksiiniga (Gram-Kopeloff)..
- Peske veega
- Laske iseenesest kuivada vertikaalses õhus.
Kui see on kuiv, asetage 1 tilk sukeldumisõli, et jälgida seda optilise mikroskoobi 100X eesmärgi all.
Utility
See meetod võimaldab eristada enamiku bakterite morfotüüpi erinevusi.
Pärmid eristuvad ka selle värvi poolest. Nad võtavad kristallvioleti, see tähendab, et nad värvivad Grami positiivset.
Teisest küljest võib eristada grampositiivseid spoore moodustavaid baktereid, kus bacilluse sees, kus endospoor tekkis, täheldatakse selget ruumi, kuigi eosed ei värvi hästi. Spooride kasutamiseks kasutatakse muid meetodeid nagu Shaeffer-Fulton.
Tuleb märkida, et see plekk ei ole mõeldud igasuguste bakterite värvimiseks, st on juhtumeid, kus värvimine ei toimi.
Sel juhul võib mainida raku seina puuduvaid baktereid. Näiteks: perekond Mycoplasma, sferoplastid, Ureaplasma, L-vormid ja protoplastid.
Samuti peitsib see halvasti mükoolhappeid sisaldavate seintega baktereid, nagu mükobakterid ja intratsellulaarsed bakterid nagu Chlamydias ja Rickettsias..
Samuti on ebatõhus enamiku spirotsetaalsete bakterite värvimine.
On samast perekonnast pärinevaid baktereid, mida võib täheldada samas proovis nagu grampositiivne ja gramnegatiivne. Kui see juhtub, nimetatakse seda muutuvaks Grami värviks, mis võib olla tingitud toitainete muutumisest, temperatuurist, pH-st või elektrolüütide kontsentratsioonist..
Üldised vead
Pleegitada liigselt
Liigutamine värvimisetapis võib põhjustada vale gramnegatiivsete mikroorganismide jälgimist.
Ärge oodake, et immersiooniõli lisamiseks oleks piisavalt kuivamisaega:
See viga põhjustab rasvaste mitsellide moodustumist, mis raskendavad olemasolevate struktuuride jälgimist. See juhtub siis, kui õli ühendab määrdeaines olevad veemolekulid.
Reagentide järjekord pööratakse tagasi:
Selline viga tekitab gramnegatiivseid baktereid purpurpunase, st vale grampositiivse.
Kasutage vanu kultuure (tahkeid või vedelaid):
See võib tekitada grampositiivseid baktereid Gram-negatiivseks (vale gramnegatiivne). See juhtub seetõttu, et vanades kultuurides on tõenäoline, et on olemas surnud või halvenenud bakterid ja neil tingimustel ei säilita bakterid lilla kristallidega.
Kasutage väga vana Lugoli lahust:
Aja jooksul kaotab lugool oma omadused ja värvus kaob. Kui kasutatakse juba degenereerunud reaktiivi, ei kinnita see kristallvioletit hästi, seega on võimalik saada mikroorganismide vale visualiseerimine Gram-negatiivse.
Sinakas taust
Õige värvusega taust on punane. Sinine taust näitab, et värvimuutus oli ebapiisav.
Viited
- Ryan KJ, Ray C. 2010. Sherris. Mikrobioloogia Medical, 6. trükk McGraw-Hill, New York, USA
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobioloogiline diagnoos. (5. väljaanne). Argentina, Redaktsioon Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Bailey & Scotti mikrobioloogiline diagnoos. 12 ed. Argentina Panamericana S.A Toimetaja
- Casas-Rincón G. 1994. Üldine mükoloogia. 2. väljaanne Universidad Central de Venezuela, raamatukogu väljaanded. Venezuela, Caracas.
- "Grami värv" Wikipedia, vaba entsüklopeedia. 4. oktoober 2018, 23:40 UTC. 9. detsember 2018, 17:11. Võetud es.wikipedia.org.
- González M, González N. 2011. Meditsiinilise mikrobioloogia käsiraamat. 2. väljaanne, Venezuela: Carabobo ülikooli meedia ja väljaannete direktoraat.
- López-Jácome L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Põhiline värvimine mikrobioloogia laboris. Puudega seotud uuringud. 2014; 3 (1): 10-18.


