Kaltsiumfosfaat (Ca3 (PO4) 2) struktuur, omadused, moodustumine ja kasutusalad
The kaltsiumfosfaat on anorgaaniline ja tertsiaarne sool, mille keemiline valem on Ca3(PO4)2. Valem ütleb, et selle soola koostis on vastavalt 3: 2 kaltsiumi ja fosfaadi puhul. Seda saab näha otse alumisest pildist, kus on näidatud Ca katioon2+ ja anioon PO43-. Iga kolme Ca kohta2+ On kaks PO-d43- nendega suhelda.
Teisest küljest viitab kaltsiumfosfaat soolade seeriatele, mis varieeruvad sõltuvalt Ca / P suhtest, samuti hüdratatsiooni ja pH tasemest. Tegelikult on olemas palju erinevaid kaltsiumfosfaate, mida on võimalik sünteesida. Kuid nomenklatuuri järgides tähendab kaltsiumfosfaat ainult eespool mainitud trikaltsiumi.

Kõik kaltsiumfosfaadid, kaasa arvatud Ca3(PO4)2, Need on valged ja kergelt hallikas toonid. Need võivad olla granuleeritud, peened, kristallilised ja nende osakeste suurused on umbes mikromeetrid; ja isegi on valmistatud nende fosfaatide nanoosakesed, millega luuakse bioloogiliselt ühilduvad materjalid.
See bioloogiline ühilduvus on tingitud asjaolust, et need soolad leiduvad hammastes ja lühidalt imetajate luukudedes. Näiteks on hüdroksüapatiit kristalne kaltsiumfosfaat, mis omakorda interakteerub sama soola amorfse faasiga..
See tähendab, et eksisteerivad amorfsed ja kristalsed kaltsiumfosfaadid. Sel põhjusel ei ole kaltsiumfosfaatidel põhinevate materjalide sünteesimisel mitmekesisus ja mitmed võimalused üllatavad; materjalid, mille omadused teadlased on rohkem huvitatud iga päev maailmas, keskendudes luude taastamisele.
Indeks
- 1 Kaltsiumfosfaadi struktuur
- 1.1 Amorfne kaltsiumfosfaat
- 1.2 Ülejäänud perekond
- 2 Füüsikalised ja keemilised omadused
- 2.1 Nimed
- 2.2 Molekulmass
- 2.3 Füüsiline kirjeldus
- 2.4 Maitse
- 2.5 Sulamistemperatuur
- 2.6 Lahustuvus
- 2.7 Tihedus
- 2.8 Murdumisnäitaja
- 2.9 Treeningu standardne entalpia
- 2.10 Hoiustamistemperatuur
- 2,11 pH
- 3 Koolitus
- 3.1 Kaltsiumnitraat ja ammooniumvesinikfosfaat
- 3.2 Kaltsiumhüdroksiid ja fosforhape
- 4 Kasutamine
- 4.1 Luukoes
- 4.2 Biokeraamilised tsemendid
- 4.3 Arstid
- 4.4 Muu
- 5 Viited
Kaltsiumfosfaadi struktuur
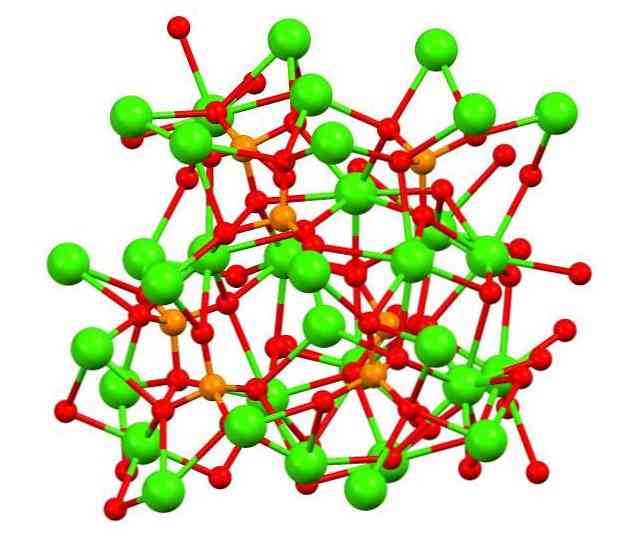
Ülemine pilt näitab tribasilise kalikoefosfaadi struktuuri kummalises valgete mineraalides, mis võivad lisandina sisaldada magneesiumi ja rauda..
Kuigi esmapilgul võib see tunduda keerukas, on vaja selgitada, et mudel eeldab kovalentset koostoimet fosfaatide hapniku aatomite ja kaltsiumi metallkeskmete vahel..
Esinduse kaudu on see kehtiv, kuid koostoimed on elektrostaatilised; see tähendab katioone Ca2+ on huvitatud PO anioonidest43- (Ca2+- O-PO33-). Seda silmas pidades on arusaadav, miks kujutises on ümbritsetud negatiivselt laetud hapniku aatomitega (punased sfäärid) kaltsiumi (rohelised sfäärid).
Kui on nii palju ioone, ei jäta see sümmeetrilist paigutust ega mustrit nähtavaks. Ca3(PO4)2 Vastab madalatel temperatuuridel (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, akronüümi eest inglise keeles).
Kõrgetel temperatuuridel aga teisendatakse see polümorfs-a-Ca3(PO4)2 (a-TCP), mille ühikrakk vastab monokliinilisele kristalsele süsteemile. Isegi kõrgematel temperatuuridel võib moodustada ka polümorfne a'-Ca3(PO4)2, mis on kuusnurkse kristallstruktuuriga.
Amorfne kaltsiumfosfaat
Kaltsiumfosfaadi kohta on mainitud kristallstruktuure, mida tuleb eeldada soolast. Siiski on see võimeline eksponeerima ebakorrektseid ja asümmeetrilisi struktuure, mis on rohkem seotud "kaltsiumfosfaadi klaasiga" kui kristallidega selle mõiste täpses tähenduses.
Kui see juhtub, siis öeldakse, et kaltsiumfosfaadil on amorfne struktuur (AKV, amorfne kaltsiumfosfaat). Mitmed autorid viitavad sellisele struktuurile, mis vastutab Ca bioloogiliste omaduste eest3(PO4)2 luukoes, selle parandamine ja biomimeerimine on võimalik.
Selle struktuuri selgitamisega tuumamagnetresonantsiga (NMR) on leitud OH ioonide olemasolu- ja HPO42- AKV riikides. Need ioonid moodustatakse ühe fosfaadi hüdrolüüsi teel:
PO43- + H2O <=> HPO42- + OH-
Selle tulemusena muutub AKV tegelik struktuur keerulisemaks, mille koostiste koostis on esindatud valemiga: Ca9(PO4)6-x(HPO4)x(OH)x. 'X' näitab hüdratatsiooni astet, kuna kui x = 1, siis oleks valem: Ca9(PO4)5(HPO4) (OH).
Erinevad struktuurid, mida PCA võib olla sõltunud Ca / P molaarsuhetest; see tähendab kaltsiumi ja fosfaadi suhtelisi koguseid, mis muudavad kogu nende saadud kompositsiooni.
Ülejäänud perekond
Kaltsiumfosfaadid on tegelikult anorgaaniliste ühendite perekond, mis omakorda võib toimida orgaanilise maatriksiga.
Teised fosfaadid saadakse "lihtsalt", muutes kaltsiumi kaasnevaid anioone (PO43-, HPO42-, H2PO4-, OH-), samuti tahke aine lisandite tüüp. Seega võib kuni üheteistkümne kaltsiumfosfaadi või rohkem, millest igaühel on oma struktuur ja omadused, pärineda looduslikult või kunstlikult..
Allpool on mõned fosfaadid ja nende vastavad struktuurid ning keemilised valemid:
-Vesinikkaltsiumfosfaadi dihüdraat, CaHPO4∙ 2H2O: monokliiniline.
-Kaltsiumdivesinikfosfaatmonohüdraat, Ca (H)2PO4)2∙ H2O: trikliiniline.
-Veevaba divesinikfosfaat, Ca (H)2PO4)2: trikliiniline.
-Occium kaltsiumvesinikfosfaat (OCP), Ca8H2(PO4)6: trikliiniline See on hüdroksüapatiidi sünteesi eelkäija.
-Hüdroksüapatiit, Ca5(PO4)3OH: kuusnurkne.
Füüsikalised ja keemilised omadused
Nimed
-Kaltsiumfosfaat
-Trikaltsiumfosfaat
-Trikaltsiumdifosfaat
Molekulmass
310,74 g / mol.
Füüsiline kirjeldus
Valge tahke aine on lõhnatu.
Maitse
Maitsetu.
Sulamistemperatuur
1670 ° K (1391 ° C).
Lahustuvus
-Vees praktiliselt lahustumatu.
-Etanoolis ei lahustu.
-Lahustub lahjendatud vesinikkloriidhappes ja lämmastikhappes.
Tihedus
3,14 g / cm3.
Murdumisnäitaja
1,629
Treeningu standardne entalpia
4126 kcal / mol.
Ladustamistemperatuur
2-8 ° C.
pH
6-8 50 g / l kaltsiumfosfaadi vesisuspensioonis.
Koolitus
Kaltsiumnitraat ja vesinik-ammooniumfosfaat
Kaltsiumfosfaadi valmistamiseks või moodustamiseks on mitmeid meetodeid. Üks neist koosneb kahe soola, Ca (NO) segust.3)2∙ 4H2O ja (NH4)2HPO4, eelnevalt lahustunud absoluutses alkoholis ja vees. Üks sool annab kaltsiumi ja teine fosfaat.
Sellest segust sadestub AKV, mida kuumutatakse seejärel ahjus temperatuuril 800 ° C ja 2 tundi. Selle protseduuri tulemusena saadakse β-Ca3(PO4)2. Temperatuuri hoolika reguleerimise, segamise ja kokkupuuteaegade korral võib tekkida nanokristallide moodustumine.
Polümorfse a-Ca moodustamiseks3(PO4)2 on vaja kuumutada fosfaati üle 1000 ° C. See kuumutamine viiakse läbi teiste metalliioonide juuresolekul, mis stabiliseerivad selle polümorfi piisavalt, et seda saaks kasutada toatemperatuuril; see tähendab, et see jääb stabiilsesse metaolekusse.
Kaltsiumhüdroksiid ja fosforhape
Kaltsiumfosfaati võib valmistada ka kaltsiumhüdroksiidi ja fosforhappe lahuste segamisel happelise aluse neutraliseerimisega. Pärast pool päeva küpsemist emalahustes ja nende nõuetekohast filtreerimist, pesemist, kuivatamist ja sõelumist saadakse amorfse fosfaadi granuleeritud pulber, AKV.
See AKV reaktsioon põhjustab kõrgeid temperatuure, muutes vastavalt järgmistele keemilistele võrranditele:
2Ca9(HPO4) (PO4)5(OH) => 2Ca9(P2O7)0,5(PO4)5(OH) + H2O (T = 446,60 ° C)
2Ca9(P2O7)0,5(PO4)5(OH) => 3Ca3(PO4)2 + 0,5H2O (T = 748,56 ° C)
Sel viisil saadakse β-Ca3(PO4)2, selle kõige levinum ja stabiilne polümorf.
Kasutamine
Luu koes
Ca3(PO4)2 See on luu tuhka peamine anorgaaniline koostisosa. See on luu asendusloomade komponent, mis on seletatav selle keemilise sarnasusega luus sisalduvate mineraalidega.
Kaltsiumfosfaadi biomaterjale kasutatakse luudefektide parandamiseks ja titaanmetallproteeside katmisel. Kaltsiumfosfaat ladestatakse neile, eraldades need keskkonnast ja aeglustades titaani korrosiooniprotsessi.
Kaltsiumfosfaadid, sealhulgas Ca3(PO4)2, Neid kasutatakse keraamiliste materjalide tootmiseks. Need materjalid on bioloogiliselt kokkusobivad ja neid kasutatakse praegu alontolaarse luu kadu taastamiseks, mis on tingitud parodondi haigusest, endodontilistest infektsioonidest ja muudest tingimustest..
Siiski tuleks neid kasutada ainult periaptilise luu parandamise kiirendamiseks piirkondades, kus ei ole kroonilist bakteriaalset infektsiooni.
Kaltsiumfosfaati võib kasutada luudefektide parandamisel, kui autogeense luu siirdamist ei ole võimalik kasutada. Seda on võimalik kasutada üksi või kombinatsioonis biolaguneva ja resorbeeruva polümeeriga, näiteks polüglükoolhappega..
Biokeraamilised tsemendid
Kaltsiumfosfaattsement (CPC) on teine biokeraamika, mida kasutatakse luukoe parandamiseks. See on valmistatud erinevate kaltsiumfosfaatide pulbri segamisel veega, moodustades pasta. Pastat saab süstida või kohandada luu defekti või õõnsusega.
Tsemendid valatakse, järk-järgult resorbeeritakse ja asendatakse vastloodud luuga.
Arstid
-Ca3(PO4)2 See on aluseline sool, nii et seda kasutatakse antatsiidina maohappe liigse happe neutraliseerimiseks ja pH suurendamiseks. Hambapastas annab see kaltsiumi ja fosfaadi allika, et hõlbustada hammaste ja luu hemostaasi remineraliseerumist..
-Seda kasutatakse ka toidulisandina, kuigi odavaim viis kaltsiumi asendamiseks on selle karbonaadi ja tsitraadi kasutamine..
-Kaltsiumfosfaati võib kasutada tetanooli, varjatud hüpokaltseemia ja säilitusravi raviks. Lisaks on see kasulik kaltsiumi lisamisel raseduse ja imetamise ajal.
-Seda kasutatakse radioaktiivsete isotoopide raadio (Ra-226) ja strontsiumi (Sr-90) saastumise raviks. Kaltsiumfosfaat blokeerib radioaktiivsete isotoopide imendumist seedetraktis, piirates seega nende tekitatud kahju.
Teised
-Kaltsiumfosfaati kasutatakse lindude söödana. Lisaks kasutatakse seda hambapastades hambakivi kontrollimiseks.
-Seda kasutatakse paakumisvastase ainena, näiteks selleks, et vältida lauasoola kokkusurumist.
-See toimib pleegitusainena jahu jaoks. Kuigi searasvas hoiab ära soovimatu värvuse ja parandab praadimise seisundit.
Viited
- Tung M.S. (1998) Kaltsiumfosfaadid: struktuur, koostis, lahustuvus ja stabiilsus. In: Amjad Z. (eds) Kaltsiumfosfaadid bioloogilistes ja tööstuslikes süsteemides. Springer, Boston, MA.
- Langlang Liu, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu ja Honglian Dai. (2018). "Nano-β-trikaltsiumfosfaadi ja hepatotsellulaarse kartsinoomi rakkude inhibeerimise süntees, iseloomustus", Journal of Nanomaterials, vol. 2018, artikli ID 7083416, 7 lehekülge, 2018.
- Combes, Kristus ja Rey, Christian. (2010). Amorfsed kaltsiumfosfaadid: süntees, omadused ja kasutus biomaterjalides. Acta Biomaterialia, vol. 6 (nr 9). lk. 3362-3378. ISSN 1742-7061
- Wikipedia. (2019). Trikaltsiumfosfaat. Välja otsitud andmebaasist: en.wikipedia.org
- Abida et al. (2017). Trikaltsiumfosfaadi pulber: valmistamis-, iseloomustus- ja tihendamisvõime. Mediterranean Journal of Chemistry 2017, 6 (3), 71-76.
- PubChem. (2019). Kaltsiumfosfaat. Välja otsitud andmebaasist: pubchem.ncbi.nlm.nih.gov
- Elsevier (2019). Kaltsiumfosfaat. Science Direct. Välja otsitud: sciencedirect.com


