Eksotermilise reaktsiooni protsess, tüübid ja näited
The eksotermiline reaktsioon on keemilise reaktsiooni tüüp, milles toimub energia ülekanne, peamiselt soojuse või valguse vabanemise vormis. Nimi pärineb Kreeka prefiksist ekso, mis tähendab "välismaal"; ja mõiste "termiline", mis viitab soojusele või temperatuurile.
Selles mõttes võivad eksotermilised reaktsioonid üle kanda teist tüüpi energiaid keskkonda, kus need tekivad, nagu plahvatused ja nende viis kineetilise ja helilise energia ülekandmiseks, kui on suurenenud gaasilises faasis kõrgetel temperatuuridel olevad ained. vägivaldselt.
Samamoodi teostatakse patareide kasutamisel ka eksotermiline reaktsioon, ainult sellisel juhul transporditakse elektrienergiat..
Indeks
- 1 Protsess
- 2 tüüpi
- 2.1 Põlemisreaktsioonid
- 2.2 Neutraliseerimisreaktsioonid
- 2.3 Oksüdatsioonireaktsioonid
- 2.4 Termiitreaktsioon
- 2.5 Reaktsiooni polümerisatsioon
- 2.6 Tuuma lõhustumise reaktsioon
- 2.7 Muud reaktsioonid
- 3 Näited
- 4 Viited
Protsess
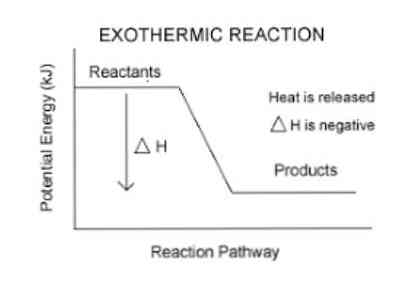
Varem mainiti, et eksotermilise reaktsiooni tekkimisel toimub energia vabanemine, mida saab hõlpsamini visualiseerida järgmises võrrandis:
Reaktiivid → Tooted + energia
Seega, süsteemi poolt absorbeeritud või vabaneva energia kvantifitseerimiseks kasutatakse termodünaamilist parameetrit, mida nimetatakse entalpiaks (tähistatud "H"). Kui süsteemis (sellisel juhul keemiline reaktsioon) on keskkonda energia eraldumine, siis entalpia variatsioonil (väljendatuna ΔH) on negatiivne väärtus.
Vastasel juhul, kui selle meetodi variatsioon on positiivne, peegeldab see soojuse imendumist ümbrusest. Samuti on süsteemi entalpiavariatsiooni suurus väljendunud keskkonnale või keskkonnast ülekantava energia kogusest..
Mida suurem on AH suurus, seda suurem on energia eraldumine süsteemist ümbritsevasse keskkonda.
Seda seetõttu, et nendes reaktsioonides on uute sidemete loomisel vabanenud netoenergia suurem kui linkide killustamisel kasutatud netoenergia..
Ülaltoodust võib järeldada, et sellised reaktsioonid on väga levinud, sest reaktsiooni produktidel on sidemetes salvestatud energia kogus, mis on suurem kui reaktiivides sisalduv energia..
Tüübid
Erinevates keemiavaldkondades eksisteerivad eksotermilised reaktsioonid nii laboris kui ka tööstuses; mõned neist viiakse läbi spontaanselt ja teised vajavad spetsiifilisi tingimusi või teatud tüüpi aineid, näiteks katalüsaatorit.
Eksotermiliste reaktsioonide kõige olulisemad tüübid on järgmised:
Põlemisreaktsioonid
Põlemisreaktsioonid on redoks-tüüpi reaktsioonid, mis tekivad siis, kui üks või mitu ainet reageerivad hapnikuga, mille tulemuseks on üldjuhul valguse ja soojusenergia vabanemine, see tähendab kerge ja soojusenergia, kui leek tekib..
Neutraliseerimisreaktsioonid
Neutraliseerimisreaktsioone iseloomustab happe liigi ja leeliselise aine (aluse) koostoime soola ja vee moodustamiseks, mis avaldavad eksotermilist laadi..
Oksüdatsioonireaktsioonid
Selliseid reaktsioone on palju, mis näitavad eksotermilist käitumist, sest hapniku oksüdatsioon põhjustab suure hulga energia vabanemist, nagu toimub süsivesinike oksüdeerimisel..
Termiitide reaktsioon
See reaktsioon võib tekitada temperatuuri umbes 3000 ° C ja alumiiniumipulbri suure afiinsuse tõttu suure hulga metalloksiididega kasutatakse seda terase ja raua keevitamisel..
Polümerisatsioonireaktsioon
Selline reaktsioon on see, mis algab siis, kui teatav arv keemilisi liike, mida nimetatakse monomeerideks, reageerivad, mis on ühikud, mida korratakse ahelates, et moodustada makromolekulaarseid struktuure, mida nimetatakse polümeeriks.
Tuuma lõhustumise reaktsioon
See protsess viitab raskeks peetava aatomi tuuma jagamisele, st massiga (A), mis on suurem kui 200), et toota väiksema suurusega fragmente või tuumasid, mille keskmine mass on.
Selles reaktsioonis, kus moodustub üks või mitu neutronit, vabaneb suur hulk energiat, kuna suurema kaalu südamiku stabiilsus on madalam kui tema toodetel..
Muud reaktsioonid
On ka teisi väga olulisi eksotermilisi reaktsioone, nagu näiteks mõnede süsivesikute dehüdratatsioon väävelhappega reageerimisel, naatriumhüdroksiidiga vee imendumine avatud õhu kätte või metalli liikide oksüdatsioon paljudes korrosioonireaktsioonides..
Näited
Allpool on mõned näited eksotermilistest reaktsioonidest, mis tekitavad entalpia variatsiooni, millel on negatiivne väärtus, kuna nad vabastavad energiat, nagu eespool mainitud..
Näiteks propaani põlemine on spontaanne eksotermiline reaktsioon:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O (l)
Teine eksotermilise käitumise juhtum on näidatud naatriumkarbonaadi ja vesinikkloriidhappe neutraliseerimisreaktsioonil:
NaHCO3(ac) + HCI (ac) → NaCl (ac) + H2O (l) + CO2(g)
Esitatakse ka etanooli oksüdeerimine äädikhappes, mida kasutatakse hingamisseadmetes, mille täielik reaktsioon on näidatud järgmises võrrandis:
3CH3CH2OH + 2K2Kr2O7 + 8H2SO4 → CH3COOH + 2Cr (SO4)3 + 2K2SO4 + 11H2O
Teine eksotermilise reaktsiooni klass on nn termiitreaktsioon, milles alumiinium kombineeritakse metallioksiidiga, nagu allpool näidatud:
2Al (s) + Usk2O3(s) → Al2O3(s) + Fe (l)
Lisaks ülalkirjeldatud näidetele on olemas ka mitmesuguseid reaktsioone, mida peetakse ka eksotermilisteks, nagu teatud orgaaniliste jäätmete lagunemine kompostimiseks..
Samuti toob see esile lutsiferiini pigmendi oksüdatsiooni lutsiferaasi ensüümi toimel, et saada paljude teiste reaktsioonide seas firefliesele iseloomulik bioluminestsents ja isegi hingamine..
Viited
- Wikipedia. (s.f.). Eksotermiline reaktsioon. Välja otsitud es.wikipedia.org-st
- BBC (s.f.). Energia muutused ja pöörduvad reaktsioonid. Välja otsitud bbc.co.uk-st
- Chang, R. (2007). Keemia, üheksas väljaanne. (McGraw-Hill).
- Walker, D. (2007). Keemilised reaktsioonid. Välja otsitud aadressilt books.google.co.ve
- Saunders, N. (2007). Keemiliste reaktsioonide uurimine. Välja otsitud aadressilt books.google.co.ve


