Joseph Thomson Biograafia ja toetused teadusele ja keemiale
Joseph John Thomson Ta oli silmapaistev keemik erinevate panuste jaoks, nagu elektroni avastamine, aatomimudel, isotoopide avastamine või katoodkiirguskatse.
Ta sündis 18. detsembril 1856 Manchesteris, Inglismaal, Cheetam Hillis. Tuntud ka kui "J.J." Thomson, õppis inseneritööd Owens College'is, mis nüüd kuulub Manchesteri ülikooli, ja hiljem, matemaatika Cambridge'is.

1890. aastal abiellus J. J. Thomson arsti Elizabeth Pagetiga, arsti Sir Edward George Pageti tütarega, kellega mul oli kaks last: tüdruk, nimega Joan Paget Thomson ja poiss George Paget Thomson.
Viimane muutuks kuulsaks teadlaseks, saades 1937. aastal Nobeli füüsika auhinna töö eest elektronidega.
Noorust alates keskendus Thomson oma aatomite struktuurile, avastades seeläbi elektronide ja isotoopide olemasolu paljude teiste panuste hulgas..
1906. aastal sai Thomson Nobeli füüsika auhinna, „tunnustades tema teoreetiliste ja eksperimentaalsete uuringute suurt väärtust elektrit läbi gaaside juhtimise”, paljude teiste tema auhindade hulgas. (1)
Aastal 1908 sõitis ta Briti krooniga ja teenis füüsika professorina Cambridge'is ja Londoni Kuninglikus Instituudis..
Ta suri 30. augustil 1940, 83, Cambridge'i linnas Ühendkuningriigis. Füüsik maeti Westminsteri kloostrisse Sir Isaac Newtoni haua lähedal. (2)
Indeks
- 1 Thomsoni peamine panus teadusse
- 1.1 Elektroni avastamine
- 1.2 Thomsoni aatomi mudel
- 1.3 Aatomite eraldamine
- 1.4 Isotoopide avastamine
- 1.5 Katoodkiirguse katsed
- 1.6 Massispektromeeter
- 2 Thomsoni pärand
- 3 Soovitatavad tööd
- 4 Viited
Thomsoni peamine panus teadusse
Elektroni avastamine
1897, J.J. Thomson avastas uue vesiniku kergema osakese, mis ristiti "elektroniga"..
Vesinikku peeti aatomkaalu mõõtmise ühikuks. Siiani oli aatom väikseim materjalijaotus.
Selles mõttes oli Thomson esimene, kes avastas negatiivselt laetud corpuscular subatomic osakesed.
Thomsoni aatomimudel
Thomsoni aatomi mudel oli struktuur, mida inglise füüsik aatomitele omistas. Teadlase jaoks olid aatomid positiivse laengu valdkond.
Seal olid negatiivselt laetud elektronid, mis olid ühtlaselt jaotunud selle positiivselt laetud pilve vahel, neutraliseerides aatomi massi positiivse laengu.
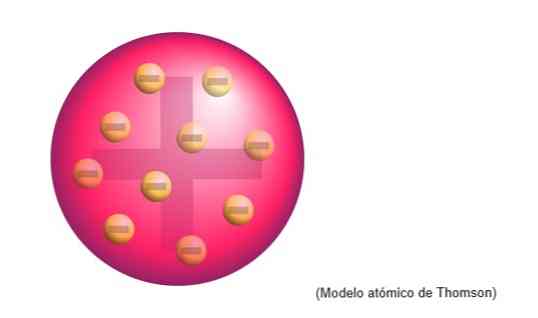
See uus mudel asendab Daltoni poolt välja töötatud mudeli ja hiljem räägib see Cambridge'i Cavendishi laborites Thomsoni jünger Rutherford..
Aatomite eraldamine
Thomson kasutas erinevate masside aatomite eraldamiseks positiivseid või anoodilisi kiire. See meetod võimaldas tal arvutada iga aatomiga transporditud elektrienergia ja molekulide arvu kuupmeetri kohta.
Erinevate masside ja laengutega aatomite jagamisel avastas füüsik isotoopide olemasolu. Ka sel moel tegi ta positiivsete kiirte uuringuga suure massispektromeetria poole.
Isotoopide avastamine
J.J. Thomson avastas, et neoonioonidel oli erinevad massid, st erinevad aatommassid. Nii näitas Thomson, et neoonil on kaks isotoopide alatüüpi: neoon-20 ja neoon-22..
Isotoopid, mida on tänaseni uuritud, on sama elemendi aatomid, kuid nende tuumadel on erinevad massinumbrid, kuna nad koosnevad erinevatest neutronite kogustest nende keskel.
Katodkiirte katsed
Katoodkiired on elektronvood vaakumtorudes, st kahe elektroodiga klaastorud, üks positiivne ja üks negatiivne.
Kui negatiivne elektrood või ka katood on kuumutatud, kiirgab see kiirgust, mis on suunatud positiivse elektroodi või anoodi suunas, kui sellel teel ei ole magnetvälja..
Kui toruklaasi seinad on kaetud fluorestseeruva materjaliga, tekitab katoodide löök selle kihi vastu valgust.
Thomson uuris katoodkiirte käitumist ja jõudis järeldustele, et kiirte levik on sirge.
Samuti, et need kiired võiksid oma trajektoorist kõrvale kalduda magnetiga, st magnetväljaga. Lisaks võivad kiirgused liigutada labasid ringleva elektronide massiga, näidates seega, et elektronidel oli mass.
J.J. Thomson katsetas katoodkiirguse sees oleva gaasi muutmist, kuid elektronide käitumine ei muutunud. Samuti soojendasid katoodkiirgused elektroodide vahele jõudnud esemeid.
Kokkuvõttes oli Thomson näidanud, et katoodkiirgustel oli valgus-, mehaaniline, keemiline ja termiline mõju.
Katoodkiiretorud ja nende valgusomadused olid transtsendentaalsed, et hiljem välja töötada toru televisioon (CTR) ja videokaamerad.
Massispektromeeter
J.J. Thomson lõi esimese lähenemisviisi massispektromeeter. See vahend võimaldas teadlasel uurida katoodkiiretorude massi / laengu suhet ning mõõta, kui palju neid magnetvälja mõju ja nende poolt ülekantava energia hulk suunavad..
Selle uurimuse tulemusel jõudis ta järeldusele, et katoodkiirte moodustasid negatiivselt laetud korpused, mis on aatomite sees, postuleerides nii aatomite jagatavust ja tekitades elektroni kuju..
Samamoodi jätkus massispektromeetria edusammud tänaseni, arenedes erinevates meetodites elektronide eraldamiseks aatomitest.
Lisaks oli Thomson esimene, kes soovitas esimene lainejuht See eksperiment koosnes elektromagnetlainete levimisest kontrollitud silindrilise õõnsuse sees, mida esmakordselt tegi 1897. aastal Lord Rayleigh, teine füüsika Nobeli preemia..
Lainejuhtmeid kasutataks tulevikus laialdaselt, isegi tänapäeval andmeedastuse ja kiudoptiliste seadmete abil.
Thomsoni pärand
Thomson (Th) loodi massispektromeetria masskoormuse mõõtmise ühikuna, mida pakkusid keemikud Cooks ja Rockwood Thomsoni auks..
See meetod võimaldab kindlaks määrata aine molekulide jaotuse vastavalt selle massile ja seda ära tundes, mis esinevad aine proovis..
Thomsoni valem (Th):

Soovitatavad tööd
- Elektri läbilaskvate gaaside laeng, elektrienergia juhtimine gaasides (1900).
- Aine corpuscular teooria, elektroni keemias ja mälestused ja peegeldused (1907).
- Peale elektroni (1928).
Viited
- Nobel Media AB (2014). J. Thomson - Biograafiline. Nobelprize.org. nobelprize.org.
- Thomson, Joseph J., Elektri juhtimine gaaside kaudu. Cambridge, University Press, 1903.
- Menchaca Rocha, Arturo. Elementaarosakeste diskreetne võlu.
- Christen, Hans Rudolf, Üld- ja anorgaanilise keemia alused, 1. köide. Barcelona, Hispaania. Ediciones Reverté S.A., 1986.
- Arzani, Aurora Cortina, Üldine elementaarkeemia. Mehhiko, toimetuse Porrúa, 1967.
- R. G. Cooks, A. L. Rockwood. Rapid Commun. Massispekter. 5, 93 (1991).


