Vee elektrolüüsi protseduur, tehnikad, mis see on, kodune katse
The vee elektrolüüs see on vee lagunemine selle elementaarseteks komponentideks elektrivoolu rakendamisega. Jätkamisel moodustuvad vesinikud ja molekulaarsed hapnikud kahele inertsele pinnale, H2 ja O2. Neid kahte pinda tuntakse paremini elektroodide nime järgi.
Teoreetiliselt on H ruumala2 moodustatud maht peab olema kaks korda suurem O-mahust2. Miks? Kuna veemolekulil on H / O suhe 2, st kaks H iga hapniku kohta. Seda suhet kontrollitakse otseselt selle keemilise valemiga, H2O. Saadud koguseid mõjutavad siiski paljud eksperimentaalsed tegurid.

Kui elektrolüüs toimub vees asuvate torude sees (ülemine pilt), vastab madalama kõrgusega vee kolonn vesinikule, kuna vedeliku pinnale avaldub suurem rõhk. Mullid ümbritsevad elektroode ja lõpuks tõusevad pärast vee aururõhu lõppemist.
Pange tähele, et torud on üksteisest eraldatud nii, et gaaside migratsioon ühest elektroodist teise on väike. Madalates kaaludes ei kujuta see endast otsest ohtu; kuid tööstusliku kaaluga, H-gaasi segu2 ja O2 See on väga ohtlik ja plahvatusohtlik.
Sel põhjusel on elektrokeemilised rakud, kus viiakse läbi elektrolüüsi, väga kallid; nad vajavad disaini ja elemente, mis tagavad, et gaasid ei seguneks kunagi, kasumlik voolutarve, suured elektrolüütide kontsentratsioonid, spetsiaalsed elektroodid (elektrokatalüsaatorid) ja mehhanismid H-i säilitamiseks.2 toodetud.
Elektrokatalüsaatorid esindavad hõõrdumist ja samal ajal vee elektrolüüsi kasumlikkuse tiibu. Mõned koosnevad väärismetallide oksiididest, nagu plaatina ja iriidium, mille hinnad on väga kõrged. Just sel hetkel eriti kui teadlased ühendavad jõud tõhusate, stabiilsete ja odavate elektroodide kujundamiseks.
Nende jõupingutuste põhjuseks on kiirendada O2, mis on antud madalamate kiirustega võrreldes H-ga2. See aeglustub elektroodi poolt, kus O on moodustunud2 see toob üldjuhul kaasa palju suurema potentsiaali rakendamise (ülepotentsiaal); mis on sama, madalama jõudluse ja kõrgemate kulude osas.
Indeks
- 1 Elektrolüüsi reaktsioon
- 1.1 Poolraku reaktsioonid
- 2 Menetlus
- 3 Tehnika
- 3.1 Elektrolüüs leeliselise veega
- 3.2 Elektrolüüs polümeeri elektrolüütilise membraaniga
- 3.3 Elektrolüüs tahkete oksiididega
- 4 Mis on vee elektrolüüsi kasutamine??
- 4.1 Vesiniku tootmine ja kasutamine
- 4.2 Silumismeetodina
- 4.3 Hapnikuga varustamine
- 5 Kodu eksperiment
- 5.1 Kodu muutujad
- 6 Viited
Elektrolüüsi reaktsioon
Vee elektrolüüs hõlmab paljusid keerulisi aspekte. Üldiselt on selle aluseks lihtne globaalne reaktsioon:
2H2O (l) => 2H2(g) + O2(g)
Nagu on täheldatud võrrandis, sekkuvad kaks veemolekuli: üks tuleb tavaliselt vähendada või saada elektronid, teine peab oksüdeerima või kaotama elektronid.
H2 See on vee vähendamise toode, sest elektronide võimendamine edendab prootoneid H+ võib olla kovalentselt seotud ja hapnik muundatud OH-ks-. Seega, H2 tekib katoodil, mis on elektrood, kus toimub reduktsioon.
Kuigi O2 tuleneb vee oksüdeerumisest, sest see kaotab elektronid, mis võimaldavad tal vesinikku siduda, ja vabastab seega prootoneid H+. O2 esineb anood, elektrood, kus toimub oksüdatsioon; ja erinevalt teisest elektroodist on anoodi ümbritsev pH happeline ja mitte alus.
Poolraku reaktsioonid
Ülaltoodud võib kokku võtta järgmiste keemiliste võrranditega poolrakkude reaktsioonide kohta:
2H2O + 2e- => H2 + 2OH- (Katood, põhi)
2H2O => O2 + 4H+ + 4e- (Anood, hape)
Kuid vesi ei saa kaotada rohkem elektrone (4e-) millest teine veemolekul võidab katoodil (2e-); seetõttu tuleb esimene võrrand korrutada 2-ga ja lahutada teise võrrandiga, et saada net võrrand:
2 (2H2O + 2e- => H2 + 2OH-)
2H2O => O2 + 4H+ + 4e-
6H2O => 2H2 + O2 + 4H+ + 4OH-
Aga 4H+ ja 4OH- nad moodustavad 4H2Või nii need kõrvaldavad neli kuuest H-molekulist2Või lahkudes kahest; ja tulemus on just ülemaailmne reaktsioon.
Poolrakkude reaktsioonid muutuvad pH väärtuste, tehnikate ja potentsiaalsete redutseerimis- või oksüdatsioonipotentsiaalidega, mis määravad, kui palju voolu tuleb tarnida, et vee elektrolüüs toimuks spontaanselt.
Menetlus
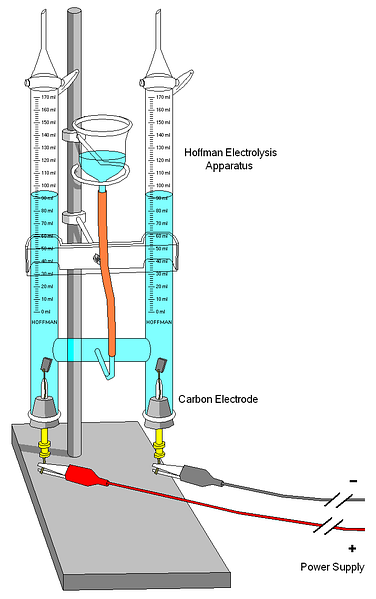
Ülemine pilt näitab Hoffmani voltmeetrit. Silindrid täidetakse veega ja valitud elektrolüütidega läbi keskmise düüsi. Nende elektrolüütide roll on vee juhtivuse suurendamine, sest normaalsetes tingimustes on väga vähe H-iioone3O+ ja OH- teie auto-ionisatsiooni tooted.
Kaks elektroodi on tavaliselt plaatina, kuigi pildil olid need asendatud süsinikelektroodidega. Mõlemad on ühendatud akuga, millega rakendatakse vee oksüdatsiooni soodustavat potentsiaalset erinevust (ΔV).2).
Elektronid liiguvad kogu ahelaga, kuni jõuad teise elektroodini, kus vesi võidab ja muutub H-ks2 ja OH-. Selles punktis on juba määratud anood ja katood, mida saab eristada veesamba kõrguse järgi; väiksema kõrgusega, vastab katoodile, kus H moodustub2.
Silindrite ülemises osas on mõned võtmed, mis võimaldavad tekkinud gaase vabastada. Te saate hoolikalt kontrollida H-i olemasolu2 selle reageerimine leegiga, mille põlemisel tekib gaasiline vesi.
Meetodid
Vee elektrolüüsi meetodid varieeruvad sõltuvalt H kogusest2 ja O2 mida soovitakse luua. Mõlemad gaasid on väga ohtlikud, kui neid omavahel segatakse, ja seetõttu on elektrolüütilistel rakkudel keerulised konstruktsioonid, et minimeerida gaasilise rõhu suurenemist ja nende difusiooni läbi vesikeskkonna..
Samuti võnkuvad tehnikad sõltuvalt rakust, veele lisatud elektrolüütist ja elektroodidest. Teisalt viitavad mõned, et reaktsioon toimub kõrgematel temperatuuridel, vähendades elektrienergia tarbimist ja teised kasutavad H-i säilitamiseks tohutut survet2 salvestatud.
Kõigist tehnikatest võib mainida kolme järgmist:
Elektrolüüs leeliselise veega
Elektrolüüs viiakse läbi leelismetallide (KOH või NaOH) aluseliste lahustega. Selle meetodiga tekivad reaktsioonid:
4H2O (l) + 4e- => 2H2(g) + 4OH-(ac)
4OH-(ac) => O2(g) + 2H2O (l) + 4e-
Nagu näha, on nii katoodil kui ka anoodil vesi aluseline pH; ja lisaks OH- migreeruda anoodile, kus nad oksüdeeruvad O-ks2.
Elektrolüüs polümeeri elektrolüütilise membraaniga
Selles meetodis kasutatakse tahket polümeeri, mis toimib H läbilaskva membraanina+, kuid veekindel gaaside puhul. See tagab suurema ohutuse elektrolüüsi ajal.
Poolrakkude reaktsioonid sel juhul on järgmised:
4H+(ac) + 4e- => 2H2(g)
2H2O (l) => O2(g) + 4H+(ac) + 4e-
H ioonid+ nad rändavad anoodist katoodini, kus nad vähendatakse H-st2.
Elektrolüüs tahkete oksiididega
Erinevalt teistest tehnikatest kasutab ta elektrolüütidena oksiide, mis kõrgel temperatuuril (600-900 ° C) toimivad anioonide transpordivahendina.2-.
Reaktsioonid on järgmised:
2H2O (g) + 4e- => 2H2(g) + 2O2-
2O2- => O2(g) + 4e-
Pange tähele, et seekord on oksiidi anioonid, OR2-, need, kes reisivad anoodile.
Mis on vee elektrolüüsi kasutamine?
Vee elektrolüüs tekitab H2 (g) ja O2 (g) Ligikaudu 5% maailmas toodetud vesinikgaasist toodetakse vee elektrolüüsil.
H2 see on NaCl vesilahuste elektrolüüsi kõrvalsaadus. Soola olemasolu hõlbustab elektrolüüsi, suurendades vee elektrijuhtivust.
Üldine reaktsioon, mis toimub, on:
2NaCl + 2H2O => Cl2 + H2 + 2NaOH
Selle reaktsiooni tohutu tähtsuse mõistmiseks mainitakse mõningaid gaasiliste toodete kasutusviise; sest lõpus on need need, mis ajendavad uute meetodite väljatöötamist, et saavutada vee elektrolüüsi tõhusam ja rohelisem viis.
Kõigist neist on kõige soovitavam olla rakud, mis asendavad energiliselt fossiilkütuste kasutamist.
Vesiniku tootmine ja kasutamine
-Elektrolüüsil toodetud vesinikku võib kasutada keemiatööstuses, mis tegutseb sõltuvushäirete, hüdrogeenimisprotsesside või redutseerimisprotsesside redutseerijana..
-Samuti on oluline, et mõnedes kaubandusliku tähtsusega tegevustes, näiteks: vesinikkloriidhappe, vesinikperoksiidi, hüdroksüülamiinide jne tootmisel. Seotud ammoniaagi sünteesiga katalüütilise reaktsiooniga lämmastikuga.
-Koos hapnikuga tekitab see kõrge kalorsusega leegid, mille temperatuur on vahemikus 3000 kuni 3500 K. Neid temperatuure saab kasutada metallitööstuse lõikamiseks ja keevitamiseks, sünteetiliste kristallide kasvamiseks, kvartside tootmiseks jne..
-Vee töötlemine: liiga suuri nitraatide sisaldust vees saab vähendada nende kõrvaldamisega bioreaktorites, kus bakterid kasutavad vesinikku energiaallikana
-Vesinik sekkub plastide, polüestri ja nailoni sünteesi. Lisaks on see klaasi tootmise osa, mis suurendab põlemisel põlemist.
-Reageerib koos paljude metallide oksiidide ja kloriidiga, sealhulgas hõbe, vask, plii, vismut ja elavhõbe, et toota puhtaid metalle.
-Lisaks kasutatakse seda leekdetektoriga kromatograafilistes analüüsides kütusena.
Silumismeetodina
Basseini vee puhastamiseks kasutatakse naatriumkloriidi lahuste elektrolüüsi. Elektrolüüsi käigus toodetakse vesinikku katoodis ja klooris (Cl2) anoodis. Sellel juhul räägitakse elektrolüüsist soolaklorinaatorina.
Kloor lahustub vees, moodustades hüpokloorhapet ja naatriumhüpokloriti. Hüdrokloorhape ja naatriumhüpoklorit steriliseerivad vett.
Hapnikuga varustamisel
Vee elektrolüüsi kasutatakse ka hapniku tekitamiseks rahvusvahelises kosmosejaamas, mis hoiab jaamas hapniku atmosfääri.
Vesinikku saab kasutada kütuseelementides, energia salvestamise meetodis ja kasutada rakus tekkinud vett astronautide tarbimiseks..
Kodu eksperiment
Laboratooriumi kaaludes on läbi viidud vee elektrolüüsi katsed Hoffmani voltmeetrite või muu seadmega, mis võimaldab elektrokeemilise elemendi kõiki vajalikke elemente sisaldada.
Kõigist võimalikest sõlmedest ja seadmetest võib kõige lihtsam olla suur läbipaistev veepaak, mis toimib rakuna. Sellele lisaks peaks teil olema käepärast ka metall- või elektrit juhtiv pind, mis toimiks elektroodidena; üks katoodi jaoks ja teine anoodi jaoks.
Selleks võivad olla kasulikud ka mõlemas otsas teravdatud grafiidipunktidega pliiatsid. Ja lõpuks, väike aku ja mõned kaablid, mis ühendavad seda improviseeritud elektroodidega.
Kui seda ei tehta läbipaistvas mahutis, ei saanud gaasimullide moodustumist hinnata.
Kodu muutujad
Kuigi vee elektrolüüs on teema, mis sisaldab palju intrigeerivaid ja lootustandvaid aspekte neile, kes otsivad alternatiivseid energiaallikaid, võib kodune katse olla lastele ja teistele pealtvaatajatele igav..
Seetõttu võib H-moodustumise tekitamiseks kasutada piisavat pinget2 ja O2 vaheldumisi teatud muutujaid ja muudatuste märkimist.
Esimene neist on vee pH varieerimine, kasutades äädikat vee hapestamiseks või Na2CO3 seda veidi leevendada. Täheldatud mullide koguse muutus peab toimuma.
Lisaks võib sama katset korrata külma ja kuuma veega. Sel viisil kaalutakse temperatuuri mõju reaktsioonile.
Lõpuks, et andmete kogumine oleks veidi vähem värvitu, võite kasutada lilla kapsamahla väga lahjendatud lahust. See mahl on loomuliku päritoluga alushappenäitaja.
Lisades selle sisestatud elektroodidega mahutisse, täheldatakse, et anoodil muutub vesi roosaks (happeks), samas kui katoodil on värvus kollane (põhi)..
Viited
- Wikipedia. (2018). Vee elektrolüüs. Välja otsitud andmebaasist: en.wikipedia.org
- Chaplin M. (16. november 2018). Vee elektrolüüs. Vee struktuur ja teadus. Välja otsitud andmebaasist: 1.lsbu.ac.uk
- Energiatõhusus ja taastuvenergia. (s.f.). Vesiniku tootmine: elektrolüüs. Välja otsitud andmebaasist: energy.gov
- Phys.org. (14. veebruar 2018). Kõrge efektiivsus, odav elektrolüüsi katalüsaator. Välja otsitud andmebaasist: phys.org
- Keemia LibreTexts. (18. juuni 2015). Vee elektrolüüs. Välja otsitud andmebaasist: chem.libretexts.org
- Xiang C., M. Papadantonakisab K. ja S. Lewis N. (2016). Elektrolüüsisüsteemide põhimõtted ja rakendused vee jagamiseks. Kuninglik Keemiaühing.
- Minnesota ülikooli Regentsid. (2018). Vee elektrolüüs 2. Minnesota ülikool. Välja otsitud andmebaasist: chem.umn.edu


